38分钟化学68页:12,下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各题.
来源:学生作业帮 编辑:搜搜做题作业网作业帮 分类:化学作业 时间:2024/08/06 18:33:48
38分钟化学68页:12,下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各题.
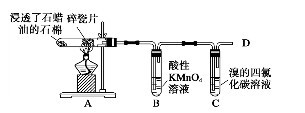
(1) 碎瓷片的作用是——
(2) B中现象是 —— ,乙烯发生—— 反应
(3) C中现象是—— ,发生反应的化学方程式 ——————————
(4) 在D处点燃时必须进行的操作是 ———— .

(1) 碎瓷片的作用是——
(2) B中现象是 —— ,乙烯发生—— 反应
(3) C中现象是—— ,发生反应的化学方程式 ——————————
(4) 在D处点燃时必须进行的操作是 ———— .

从碎瓷片的位置可以看出,碎瓷片处在酒精灯的火焰处,所以其作用主要是催化(题中也有涉及,炽热的碎瓷片下石蜡油分解).
乙烯可以被KMnO4氧化,生成CO2,所以B中的现象为高锰酸钾溶液的紫红色褪去.
反生的反应是氧化反应.
由于乙烯中含有一个不饱和的双键,可以和溴进行加成反应,溴的四氯化碳溶液为橙红色(比溴水的颜色要深一些),现象是橙红色褪去,变为无色.
反应式:CH2=CH2+Br2 → CH2Br-CH2Br
D处点燃时,需要进行验纯操作.验纯也是点燃每个可燃的气体前所必须要做的一步.
这道题的核心在于乙烯的化学性质,主要就是双键的性质.可被加成,可被氧化.最后一个验纯涉及到实验操作步骤的考察.
乙烯可以被KMnO4氧化,生成CO2,所以B中的现象为高锰酸钾溶液的紫红色褪去.
反生的反应是氧化反应.
由于乙烯中含有一个不饱和的双键,可以和溴进行加成反应,溴的四氯化碳溶液为橙红色(比溴水的颜色要深一些),现象是橙红色褪去,变为无色.
反应式:CH2=CH2+Br2 → CH2Br-CH2Br
D处点燃时,需要进行验纯操作.验纯也是点燃每个可燃的气体前所必须要做的一步.
这道题的核心在于乙烯的化学性质,主要就是双键的性质.可被加成,可被氧化.最后一个验纯涉及到实验操作步骤的考察.
38分钟化学68页:12,下面是石蜡油在炽热碎瓷片的作用下产生C2H4并检验C2H4性质的实验,完成下列各题.
实验室石蜡油在炽热碎石片的作用下产生C2H4并检验其性质中通入溴的四氯化碳的化学方程式
石蜡油分解制烯烃的实验 碎瓷片的作用
某学生根据石蜡油在碎瓷片或氧化铝催化作用下能分解得到乙烯2性质,设计如图2实验装置.据图回答:
在石蜡油制取乙烯实验中,碎瓷片其催化作用?装载它的试管是否一定要平放?
石蜡油蒸汽与炽热的碎瓷片表面反应,生成的气体通到溴的CCL4溶液中,什么现象
石蜡油分解实验 碎瓷片作用 为什么是 催化功能 和积蓄热量?
在标准状况下,C2H4和CO混合气体100 L,充分燃烧时耗用等体积的O2,则CO与C2H4的体积比是:
鉴别并检验so2 co2 c2h4
在标准状况下,1体积的C2H4和C2H2的混合气体在催化剂作用下,恰好与1.7体积的H2
下列2种气体的分子数一定相等的是A质量相等,密度不等的N2,C2H4 B等体积,等密度的CO,C2H4
高一化学题:C2H4和O2的混合物密度相当于同状态下的H2的14.5倍,求C2H4在混合物中的质量分数